Atom ve Atomun Yapısı – Özellikleri – Modeli
Atom nedir: Birçok alt parçacığı olan ve maddenin en küçük yapı taşına denir. Bir elementin bütün özelliğini taşıyan en küçük parçasıdır. Atom gözle görülmesi imkânsız, çok küçük bir parçacıktır. Sadece tünel mikroskobu (atomik kuvvet mikroskobu) ile incelenebilir.
Eski Yunan filozofları maddenin olabilecek en küçük halinin maddenin yapıtaşı olduğunu düşünmüşlerdir. Bu yapıya Yunanca’ da kesilemez, bölünemez anlamına gelen atom adını vermişlerdir.
Bir atomda, çekirdeği saran negatif yüklü bir elektron bulutu vardır. Çekirdek pozitif yüklü protonlar ve yüksüz nötronlardan oluşur. Nötronlar daha çok nötr olan yapılardan oluşmaktadır. Bunların hiçbir şekilde bir yükü bulunamamaktadır. Proton ise pozitif çekici özelliği olan bir yapıdır. Elektron ise negatif yüklü yapılardan oluşmaktadır.
Atom tüm maddenin kimyasal ve fiziksel niteliklerini taşır. Maddeyi oluşturan atomlar sürekli olarak hareket ederler.
Atomun Yapısı
Atom yapısının içerisinde daha küçük parçacıklar bulunmaktadır. Daha ufak parçacıklar nötron, proton ve elektrondur. Atomun çekirdeğinde proton ve nötron, elektron ise çekirdeğin etrafında itme ve çekme hareketleri sonucunda dönmektedirler. Bunların dönmesi halinde itme ve çekme kuvvetleri sayesinde asla bir biri ile çarpışmamaktadır. Elektronlar çok geniş bir alanda bulunmaktadırlar.
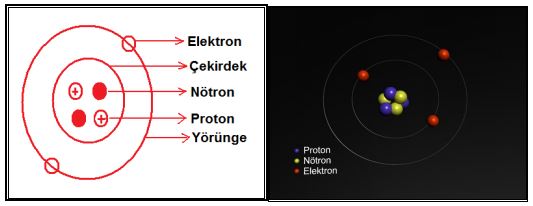
Atomu oluşturan parçacıklar farklı yüklere sahiptir. Bu yükler; negatif ve pozitif yüklerdir.
- Cisimden cisme elektrik yüklerini taşıyan negatif yüklü elektron,
- Elektronların yükünü dengeleyen aynı sayıda ama pozitif yüklü olan proton,
- Elektrik yükü taşımayan nötr parçacık nötron.

Atomun yapısı
Atomun, değişik durumlarda ortaya çıkan bir çok parçacıkları vardır. Bunlar; Positon, Meson, Neutrino, Deuteron, Triton, Alfa zerrecikleri, Gama ışınları.
Atom iki bölümden oluşur;
- Çekirdek (merkez)
- Katmanlar (yörünge; enerji düzeyi)
1. Atom Çekirdeği
Atomun tüm kütlesini oluşturan çekirdek, hacim olarak küçüktür. Çekirdekte proton ve nötronlar vardır. Elektronlar ise çekirdek çevresindeki katmanlarda bulunur. Atomun çekirdeğinde yer alan nötronlar yüksüz, protonlar ise (+) elektrikle yüklüdür. Her atomun çekirdeğinde en az bir proton yer alır. Nötron ise çekirdeğinde birden fazla proton bulunan atomlarda bulunur. Çekirdekteki proton sayısına, o atomun atom numarası denir.
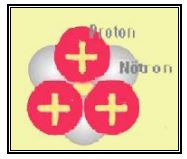
Proton sayısı o elementin atom sıra numarasını gösterir. Çekirdekteki nötron ve proton sayılarının toplamı o maddenin atom ağırlığı (kütle numarası) demektir. Çekirdek atomun merkezinde bulunur. Çekirdek belli sayıda proton ve nötrondan oluşmuştur.
Çekirdeğin yarıçapı, atomun yarıçapının on binde biri kadardır. Kuantum mekaniği yasalarının geçerli olduğu birçok sistem gibi çekirdek de anlaşılması zor ve gizemlidir. Bir atomun çekirdeği proton ve nötrondan oluşur.
Çekirdekteki proton ve nötronlara ortak olarak nükleon denir. Kütle numarası (K x N) atom numarası (A x N) ile elementin atom numarası Z ile gösterilir. Çekirdekteki nötron sayısı N ile gösterilirse A = Z + N olur.
| Tanecik adı | Sembol | Elektrik yükü | Kütle kg |
| Proton | P+ | + | 1,6725.10-27 kg |
| Elektron | e¯ | – | 9,107.10-31 kg |
| Nötron | n0 | 0 | 1,6748.10-27 kg |
Elektronların çekirdek çevresinde dönme hızı, 2,18.108 cm / sn’ dir. Elementlerin çekirdekte bulunan protonlar, atomun (o elementin) tüm kimyasal ve fiziksel özelliklerini belirler.
Proton
Atomun çekirdeğini oluşturan elemanlardır. Protonlar pozitif elektrik yüklü parçacıklardır. Elektronların yükünü dengeler. Protonun ağırlığı; elektrondan fazladır. Sadece taşıdığı elektrik yükünün miktarı elektron ile aynıdır.
Atomların cinslerine göre çekirdeklerindeki proton sayısı değişmektedir. Bu da atomlar (elementler) için ayırt edici özelliktir. Yani proton sayısının farklı olması elementin diğerinden farklı olduğu anlamına gelir.
Nötron
Nötron, elektrik yükü olmayan nötr parçacıktır. Atom çekirdeklerinde nötronlar vardır. Protondan daha ağırlardır. Nötronların sayıları atomun cinsine göre değişmektedir.
Elektron
Elektronların bulunma olasılığının olduğu bölgelere elektron bulutu denir. Merkezde atom çekirdeği bulunur. Elektronlar tek tek bulut oluştururlar. Elektron bulutu bir küre meydan getirir. Kimyasal olaylarda (reaksiyonlarda) yalnızca elektron sayısı değişir. Proton ve nötron, çekirdekte bulunduğu için sayıları değişmez.
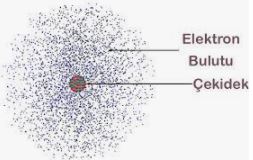
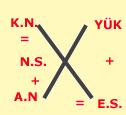
- Nötr bir atom için; elektron sayısı= proton sayısı
- (A.N.) Atom numarası= proton sayısı
- Çekirdek yükü= proton sayısı
- İyon yükü= proton sayısı – elektron sayısı (E.S.)
- (K.N.) Kütle numarası= proton + (N.S)nötron sayısı (Nükleon sayısı)(atom ağırlığı)
- Atom Numarası = Proton Sayısı = Çekirdek Yükü = Elektron Sayısı
İzotop Atom Nedir?
Atom numarası (proton sayısı) aynı, ama kütle numarası (atom ağırlığı) ise farklı olan atomlara, “izotop” denir. Diğer bir ifadeyle proton sayıları aynı (p x s= A x N), nötron sayısı (K x N = p x s + n x s) farklı atomlara izotop atom denir.

Bir atomun proton sayısı atom numarasını; proton ve nötronların toplamı ise kütle numarasını anlatır. Bir elementin farklı sayıda izotopu olabilir. Bu izotoplar, farklı kütle numarasına sahiptir. İzotopların nötron sayıları farklıdır.

Atomların kimyasal özellikleri, yörüngedeki elektronların durumuna bağlıdır. Bundan dolayı elektron dizilişleri eşit olan atomların tüm kimyasal özellikleri de aynıdır. Dengeli atomlarda proton sayısıyla elektron sayısı birbirine eşittir.
Çekirdeklerinde eşit sayıda proton olan atomlar, nötron sayıları farklı olsa bile kimyasal özellikleri aynıdır. Dolayısı ile bir elementin bütün izotopları aynı kimyasal özellikleri taşır. Ancak; izotopların fiziksel özelliklerini nötronların sayısı belirler. Bundan dolayı izotopların fiziksel özellikleri farklıdır.
Kimyasal özellikleri aynı, atom ağırlıkları farklı atomlar, birbirinin izotopu durumundadır. İzotopların atom ağırlıklarının farklı olması, bu atomların çekirdeklerindeki nötron sayılarının farklı olmasındandır.
Bazı izotoplar radyoaktif değildir. Oysa bazı izotoplar ise radyoaktiftir. Elementlerin atom numaraları arttıkça, izotop sayıları da artar. Bir izotop, radyoaktif özellik taşıyorsa “radyoaktif izotop” adını alır. Aynı elementin doğal ve yapay radyoizotopu aynı özellikleri taşır.
2. Atomun Yörüngesi (Katmanlar; Enerji Düzeyi)
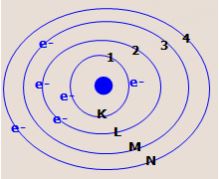
Atomda yörüngeler içten dışa doğru K,L,M,N,O,P ve Q şeklinde sıralanmış olup her yörüngenin enerji seviyesi birbirinde farklıdır. Elektronların çekirdek etrafında bulunur. Elektron hareket ettiği enerji seviyelerine katman denir. Elektron katmanlarına enerji düzeyi de denir.
Bütün atomların dış bölümü elektron katmanlarından oluşur. Her katman çekirdekten uzaklığına göre K, L, M. gibi harflerle adlandırılmaktadır. Atomun etrafında katman katman yörüngeler vardır. Atomda yörüngeler içten dışa doğru K,L,M,N,O,P ve Q şeklinde sıralanmış olup her yörüngenin enerji seviyesi birbirinde farklıdır.
Bu yörüngelerde elektronlar bulunur. Yörünge “n” harfi ile gösterilir.

Yörüngede olan en fazla elektron sayısı 2n2 formülü ile bulunur.
aX: a, X atom numarasını gösterir.
Bunlar K, L, M, N,… gibi harflerle gösterilirken aynı zamanda 1, 2, 3, 4,… gibi numaralarla da gösterilir. Bu numaralara baş kuantum sayısı adı verilir. Yörüngelerinde kendi içlerinde alt birimleri vardır. Bunlara orbital adı verilir.
İletken ve Yalıtkan Nedir?
Elementlerin özelliklerini atomların son yörüngesindeki elektron sayıları belirlemektedir. Elektrikte kullanılan maddelere; yalıtkan, iletken, yarı iletken madde denir.

İletken Nedir?
Atomları elektron vermeye yatkın olan maddelerde, serbest elektron sayısı fazladır. Elektron almaya yatkın olanlarda ise serbest elektronlar azdır. Dış yörüngelerindeki elektron sayısı dörtten az olan atomların serbest elektron sayısı fazladır. Serbest elektronu fazla maddeler, elektrik akımını kolaylıkla iletirler. Elektrik akımını iyi ileten maddelere, iletken denir.

İletken malzemelerde örneğin; Bütün metaller gümüş, bakır ve alüminyum gibi maddeler iletkendir. Bunlar serbest elektronlardır. İletkenler üzerindeki serbest elektronlar elektrik akımını bir noktadan bir noktaya kolaylıkla taşırlar.
Vücudumuzda iyi bir iletkendir. İyonlara sahip sıvılar da iletkendir, bunlara elektrolit denir. İçtiğimiz su iletken, saf su yalıtkandır. Toprağın içinde su olduğundan iletkendir. Gazlar ise yalıtkandır. Fakat iyonlarına ayrışan gazlar iletkendir.
Yalıtkan
Atomlarının son yörüngelerinde beş ve daha fazla elektron bulunduran maddelere yalıtkan denir. İçinde serbest elektron bulunmayan ve elektrik akımını iletmeyen maddelere denir. Dış yörüngelerindeki elektron sayısı dörtten fazladır.
Elektron sayıları 5-6-7 olan elementler ise bir yere kadar yalıtkan sayılır. Yalıtkan maddelerde serbest (valans) elektronlar çok azdır. Kauçuk, kağıt, hava, yağ, tahta, teflon, plastik, porselen, ebonit, mika, bakalit, cam yalıtkan maddelerdir. Kendimizi bu maddelerle yüksek gerilimin etkilerinden koruyabiliriz. Ayrıca saf su, alkol, şekerli su da yalıtkan maddelerdir.

Değerlik elektronları atomlara sıkıca bağlanmıştır. Bu malzemelerde elektronlar hareket etmezler. Bu maddelerin değerlik elektron sayıları 8 veya 8 ‘e yakın sayıda olduğu için atomdan uzaklaştırılmaları zordur.
Yarı İletken
Elektrik iletkenliği, iletken ve yalıtkanlar arasında bulunan maddelere denir. Bu maddeler düşük sıcaklıkta yalıtkan; yüksek sıcaklıkta iyi bir iletkendir. Uygulanan akım veya da gerilimle iletkenlik değişir. Yarı iletkenlik entegre devre, diyot ve transistör devre elemanlarının yapımında kullanılır. Örneğin germanyum, silisyum gibi maddeler yarı iletkendir.
Elektrik Yükü ve Birimi
Atomun yapısını proton ve elektronlar oluşturmaktadır. Proton ve elektronların elektriksel özellikleri birbirlerine tezattır. Proton (+) yüklü, elektron (-) yüklüdür. Nötronlarsa yüksüzdür. Elektrik yükü Q ya da q ile, birimi coulomb ise C ile gösterilmektedir. Proton ve elektron sayıları bir atomda eşit ise bu atoma nötr atom denir.
Atoma elektron verilerek ya da atomdan elektron alınarak atomların yüklenmesi sağlanır. Bir atomda proton sayısı elektron sayısından fazla ise bu atomlara pozitif yüklü iyon veya katyon denir. Simgesi “+e” ile gösterilmektedir.
Atomun içinde elektron sayısı çoksa dışarıdan elektron kazanmıştır. Buna negatif yüklü iyon denir ve “– e” ile gösterilir. Aynı zamanda bunlara “anyonda” denir.
(aX ±b) ifadesinde;
- A: X atomunun atom numarasını,
- +b: X atomunun kaybetmiş olduğu elektron sayısını,
- -b: X atomunun kazanmış olduğu elektron sayısını gösterir.
Atom Ağırlığı
Farklı atomlardaki protonlarla neutronların sayısına “atom sayısı” ve “atom ağırlığı” adı verilir. Bir atom sayısı, o atomda ne kadar proton, yada elektron bulunduğunu gösterir. Bu durumda, o atomun hangi elemanının atomu olduğu anlaşılır.
Atom Modelleri
Atom ve atomun yapısı üzerine tarih boyunca ortaya atılmış birçok fikirler bulunmaktadır. Eksi yüklü parçacıkların (elektronlar) artı yüklü kütle içinde sabit durduğu, üzümlü keki andıran Thomson’ un tarifi. Sonrasında bu parçacıkların kekin üzümleri gibi homojen dağılmadıklarını gösteren Rutherford’ un modeli. Bugün birçoğumuzun kafasındaki atom görüntüsünü tarif eden Danimarkalı fizikçi Niels Bohr’ un modeli. Bu fikirlere birer örnek olarak gösterilebilir.
BENZER YAZILAR





ellerine saglık
Teşekkürler
İYİ idââre eder!!!!!!
çok uzun ama harika ellerinize sağlık….☻
Proje Ödevimde Çok Yardımcı Oldu. Teşekkürler
masallah co guzel anlatmıs bayıldım
çok güzel ellerinize sağlık sizin sayenizde ödevimden 100 aldım
Çok ama çok güzel dönem performans ödevim için araştırma yapıyordum burayı bulduğuma sevindim çünkü detayları çok güzel anlatılmış elinize sağlık
Çok güzel anlatmışsınız ellerinize sağlık